近日,由四川大学华西医院生物治疗国家重点实验室与癌症中心主导,联合重庆市健康资源创新研究院、成都血液中心、四川省人民医院、西部战区总医院等多个机构合作完成并发表于《Cell Reports Medicine》的一项研究创新性地开发出了一款基于纳米抗体的三特异性NK细胞衔接器1H6-15-NKCE,为解决T细胞恶性肿瘤治疗瓶颈提供了全新方案。该研究成功筛选出高亲和力抗CD5 scFv和特异性抗CD16a纳米抗体(P60),构建双特异性NK细胞衔接器1H6-NKCE,该分子可高效激活NK细胞,杀伤CD5+肿瘤细胞。进一步融合IL-15Rα/IL-15复合物构建的三特异性衔接器1H6-15-NKCE,显著增强NK细胞增殖、存活及细胞毒性,体内外实验均展现出强效抗肿瘤活性,并且未观察到针对正常T细胞的“脱靶毒性”,安全性与疗效均优于CD5-CAR-T疗法。让我们一起来详细解读这项突破性的研究吧。
抗CD5 scFv与抗CD16a纳米抗体的筛选及鉴定
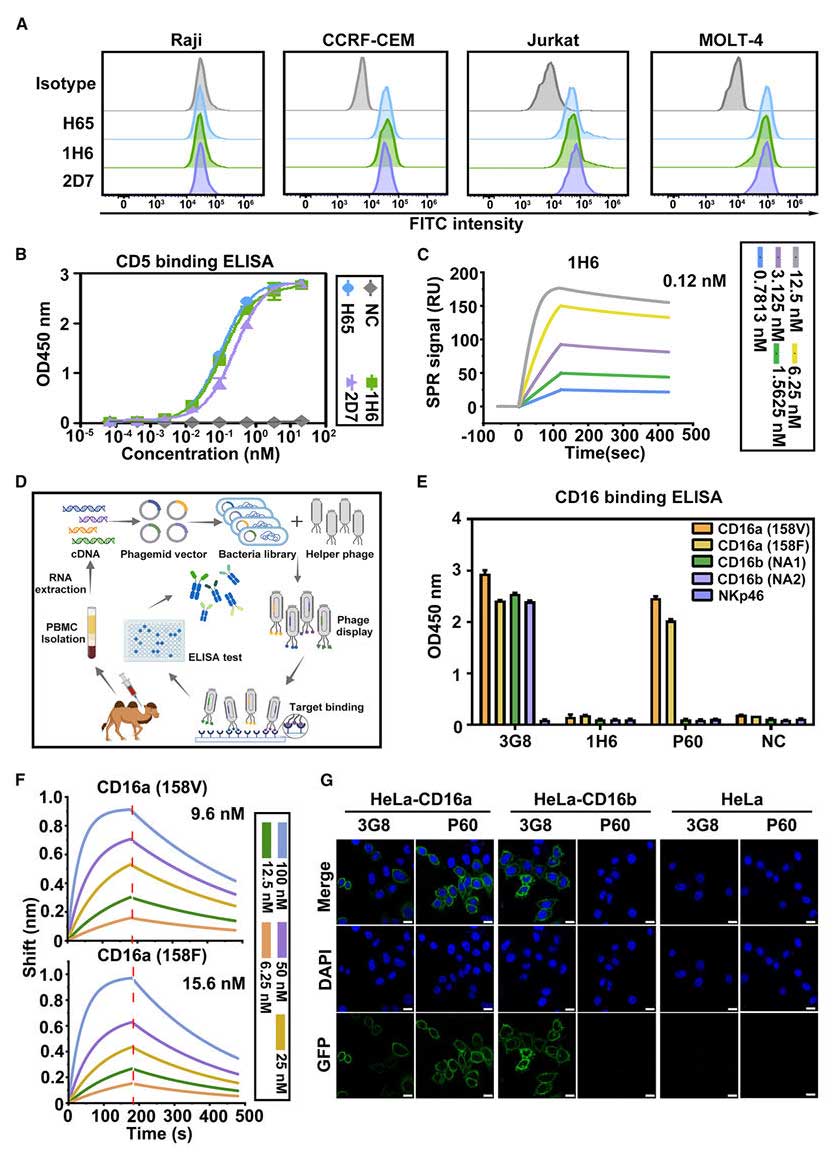
研究团队首先通过小鼠免疫与杂交瘤技术,获得4株抗CD5阳性克隆,将其重链可变区(VH)与轻链可变区(VL)通过(G₄S)₃ linker连接形成scFv,并与人类IgG4 Fc融合表达。流式细胞术与酶联免疫吸附试验(ELISA)显示,克隆1H6对CD5+肿瘤细胞的结合特异性与亲和力显著优于2D7,SPR测定显示1H6具有高亲和力(KD=1.02 nM)。
为获得特异性结合CD16a的纳米抗体,研究团队用CD16a胞外域免疫羊驼,构建重链可变区(VHH)噬菌体文库,经4轮淘选后,筛选出仅结合CD16a而不结合CD16b的克隆P60。BLI实验证实了P60对CD16a的特异性结合,亲和力达9.6nM(158V)和15.6nM(158F),而与CD16b无结合,从而避免了因结合CD16b可能引发的体内副作用。
图1:抗CD5 scFv及抗CD16a纳米抗体筛选与表征
双特异性NK衔接器1H6-NKCE的构建与体外活性验证
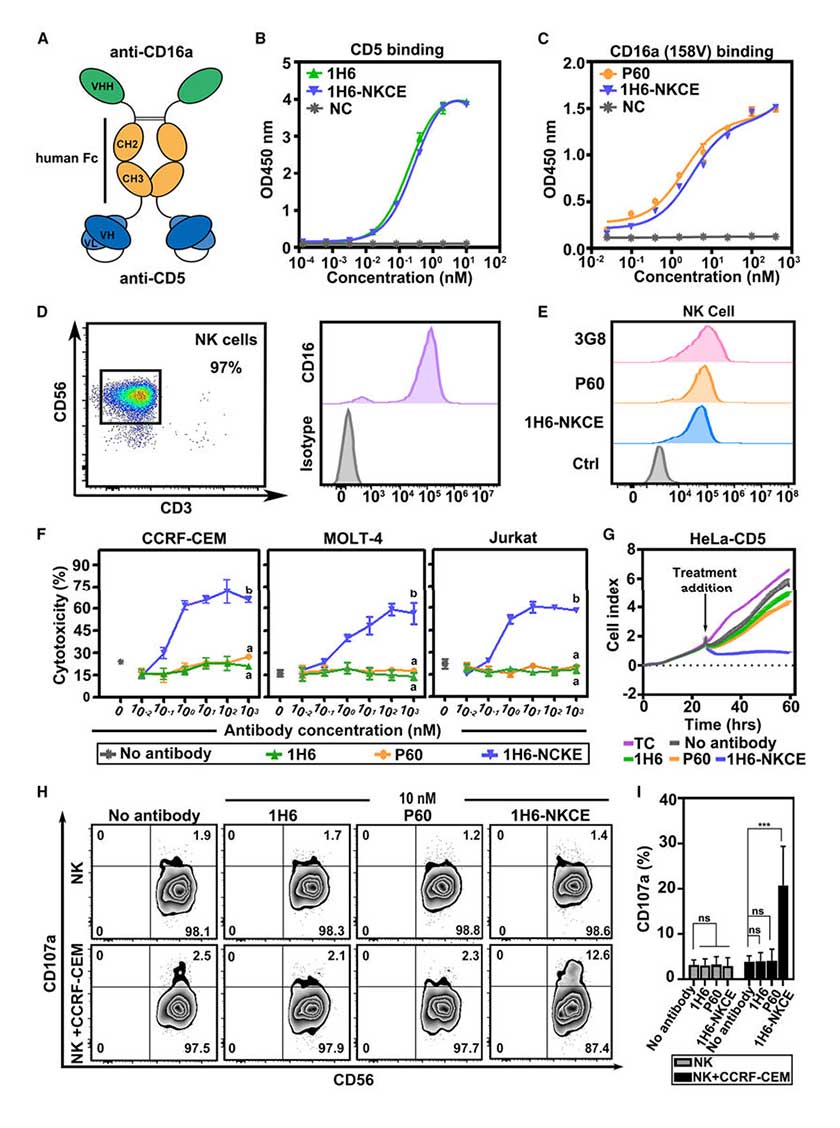
研究团队将抗CD16a纳米抗体P60与抗CD5 scFv通过人IgG4 Fc进行连接,构建双特异性衔接器1H6-NKCE,SDS-PAGE证实其正确表达与纯化。ELISA与BLI验证显示,1H6-NKCE可同时结合CD5和CD16a(158V/F),且不结合CD16b。
体外杀伤实验表明,1H6-NKCE可显著激活NK细胞,其对于CCRF-CEM、MOLT-4、Jurkat等CD5+肿瘤细胞的杀伤活性显著高于单独使用1H6或P60,而对CD5-的Raji细胞无杀伤作用。实时细胞分析显示,1H6-NKCE在60小时内持续杀伤HeLa-CD5细胞,且对未转染CD5的HeLa细胞无作用,证实其杀伤特异性。CD107a脱颗粒实验显示,1H6-NKCE处理后CD107a+NK细胞比例显著升高,RNA测序分析表明,经1H6-NKCE处理的NK细胞中,与II型干扰素反应、TNF-α信号通路及非经典NF-κB通路相关的基因集显著富集。
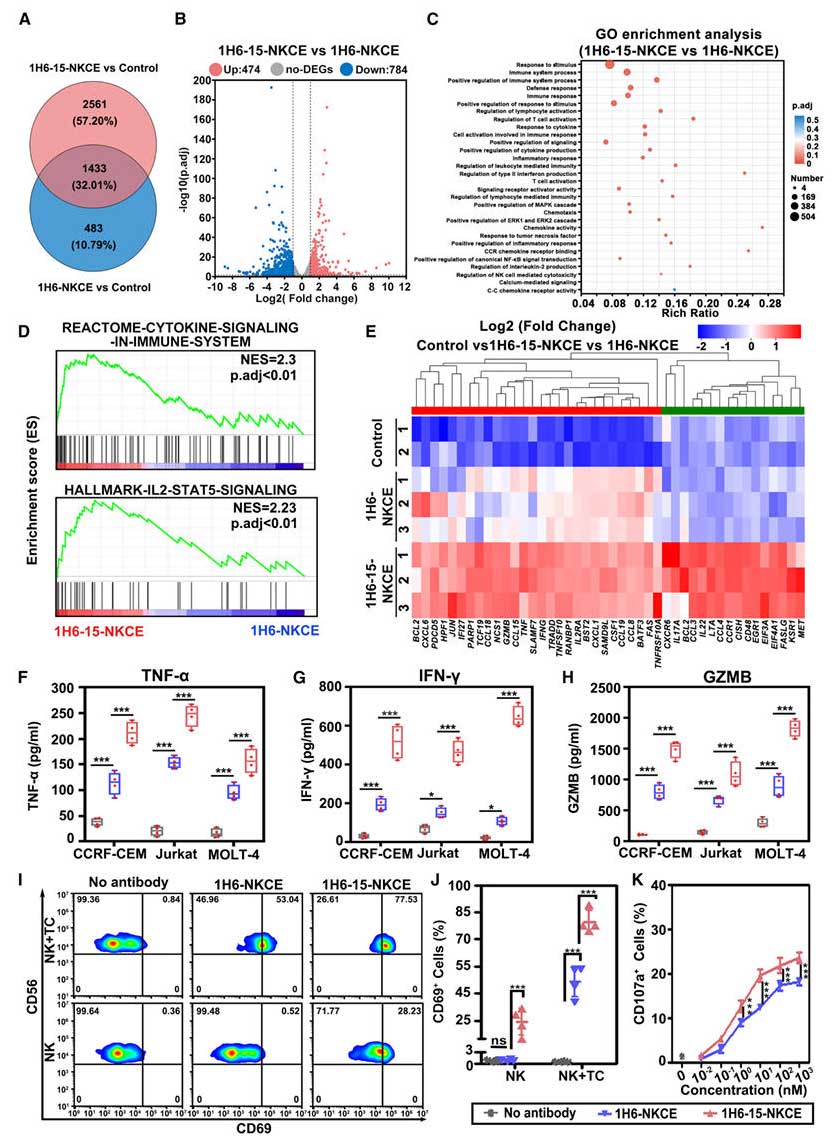
图2:1H6-NKCE的体外活性
三特异性衔接器1H6-15-NKCE的构建与功能增强验证
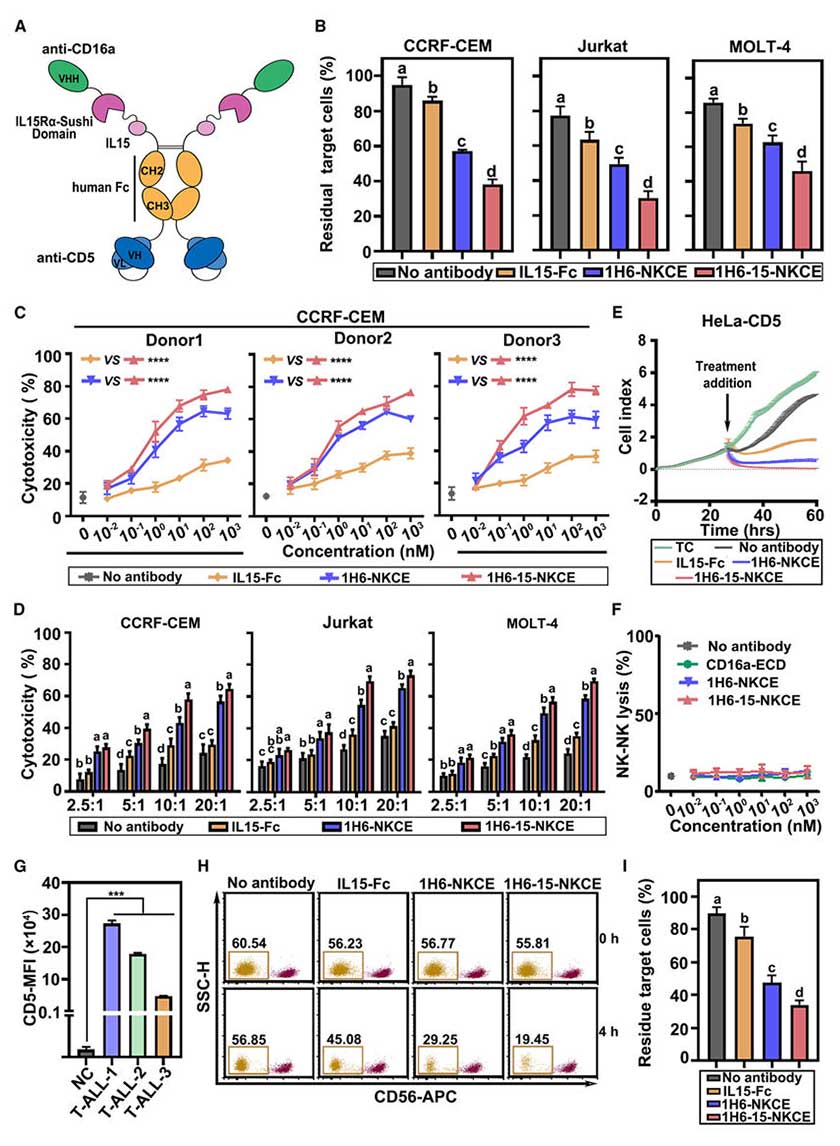
鉴于IL-15可增强NK细胞增殖、存活与细胞毒性,且避免调节性T细胞介导的免疫抑制,团队将可溶性IL-15Rα sushi结构域与IL-15形成的复合物融合至1H6-NKCE的C端,构建三特异性衔接器 1H6-15-NKCE,SDS-PAGE与ELISA证实其正确表达且含功能性IL-15。
体外实验显示,1H6-15-NKCE处理后,残留CD5+肿瘤细胞比例显著低于1H6-NKCE与IL-15-Fc处理组。对不同供体来源的NK细胞,1H6-15-NKCE均能显著增强其对CD5+肿瘤细胞的杀伤活性,且在效应细胞与靶细胞(E:T)比例为10:1时效果最显著。RTCA显示,1H6-15-NKCE激活的NK细胞对HeLa-CD5细胞的长期杀伤效果优于1H6-NKCE,且未观察到NK细胞自相残杀(fratricide)现象。对3例CD5+原发性T-ALL样本,1H6-15-NKCE介导的异源及自体NK细胞均展现更强的肿瘤清除能力。
图3:1H6-15-NKCE对NK细胞的功能增强
1H6-15-NKCE的作用机制与细胞安全性验证
转录组分析显示,与1H6-NKCE相比,1H6-15-NKCE处理的NK细胞中,免疫反应、细胞因子信号、趋化等通路显著富集,JAK/STAT通路因IL-15信号激活而上调,IFN-γ、GZMB、TNF等细胞因子分泌量显著增加。CD69激活标志物与CD107a脱颗粒标志物检测证实,1H6-15-NKCE可更强地激活NK细胞。
图4:转录组学机制分析与1H6-15-NKCE相关
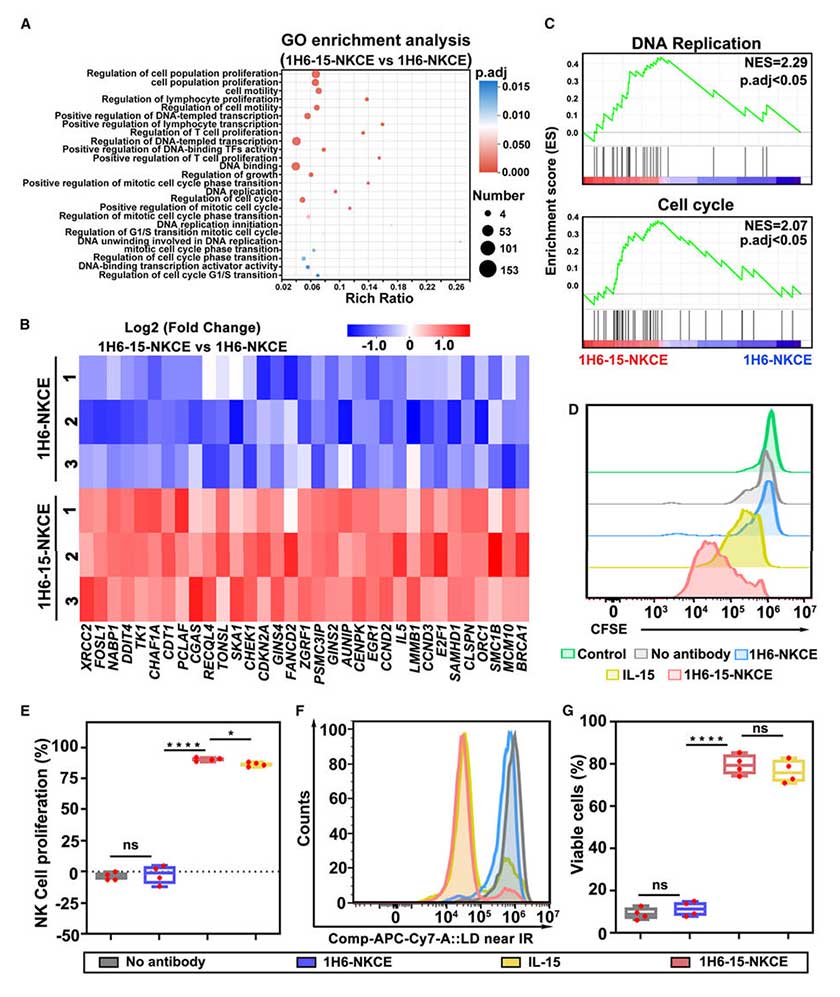
增殖实验显示,与1H6-NKCE或单独IL-15处理相比,1H6-15-NKCE能更有效地诱导NK细胞增殖,在培养7天后显示出更高的增殖比例与细胞存活率,且仅激活正常T细胞增殖,不促进CD5+肿瘤细胞增殖。
图5:1H6-15-NKCE有效诱导NK细胞存活与增殖
体内抗肿瘤活性与安全性验证
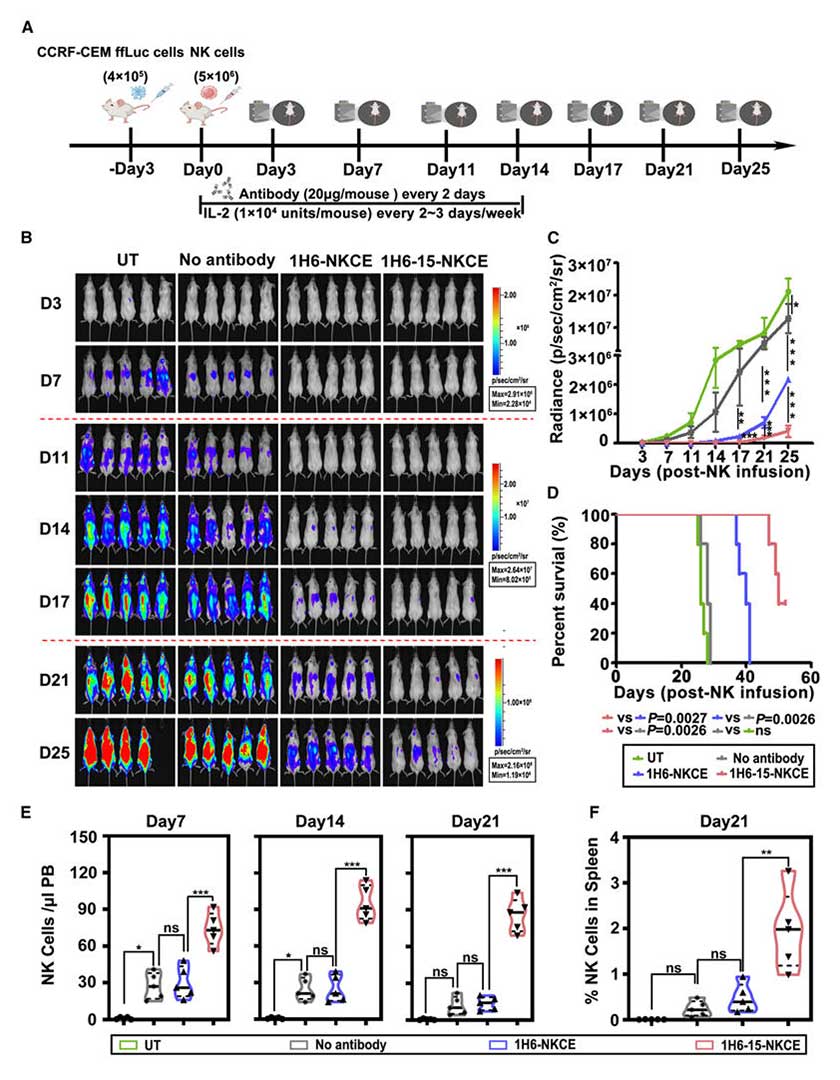
在CCRF-CEM-ffLuc异种移植模型中,1H6-15-NKCE联合NK细胞治疗组的肿瘤负荷显著低于1H6-NKCE组,中位生存期从40天延长至 50天(p<0.01),外周血与脾脏中NK细胞数量显著增多,证实其可增强NK细胞体内持久性。
图6:1H6-15-NKCE的抗肿瘤活性
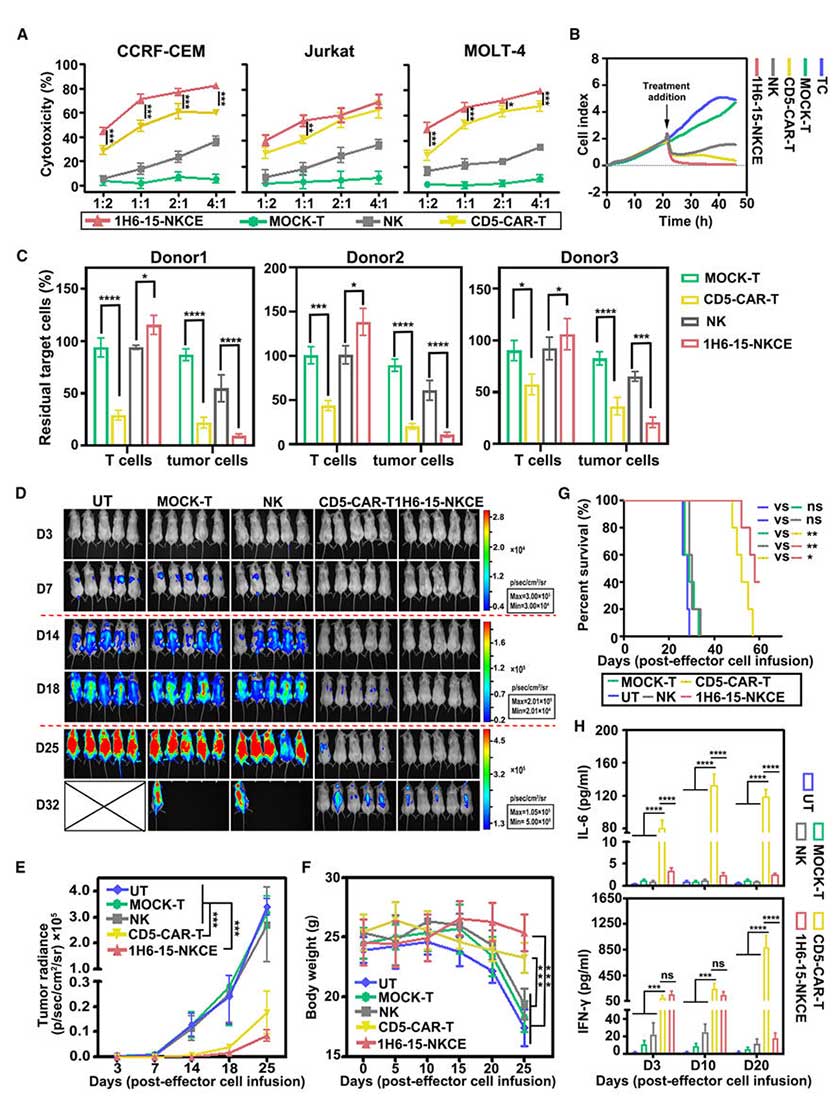
与CD5-CAR-T疗法对比,1H6-15-NKCE激活的NK细胞在体外对 CD5+肿瘤细胞的杀伤活性相当,但对正常自体T细胞无毒性,而CD5-CAR-T细胞会同时杀伤正常T细胞与肿瘤细胞。在MOLT-4-ffLuc异种移植模型中,1H6-15-NKCE联合NK细胞治疗组与CD5-CAR-T治疗组均显著抑制肿瘤生长,但1H6-15-NKCE组小鼠体重无明显下降,血清中IL-6水平较低,提示其引发细胞因子释放综合征的风险较低,且 2/5小鼠在60天仍存活,疗效与安全性更优。
图7:CD5-CAR-T & 三特异性NK细胞抗肿瘤活性对比
该研究不仅成功开发了一种具有高度转化潜力的三特异性NK细胞衔接器,更凸显了纳米抗体在下一代免疫治疗中的核心价值。1H6-15-NKCE以其精准的靶向能力、强大的NK细胞激活效应以及卓越的安全性,为T细胞恶性肿瘤的治疗开辟了一条全新路径,也为全球免疫治疗领域注入了新的创新动力。

武汉纳博生命科技有限公司是由武汉产业创新发展研究院牵头成立建设的纳米抗体产业平台。其总部位于武汉东湖新技术开发区武创院本部大楼,在武汉生物城精准医疗产业基地拥有占地面积达1400㎡的自主实验室,并在武汉左岭与黄冈团风分别建立了符合实验动物标准的羊驼实验基地与转运基地,目前基地在饲养的羊驼共600余头,可为科研机构及抗体药物研发企业提供“零免疫背景”保障的羊驼免疫服务。
纳博生命专注于纳米抗体开发、改造与应用,致力于构建产、学、研一体化的实验公共服务平台。现拥有从抗原制备(多肽、蛋白及RNA),到抗体发现和抗体工程,再到生物学功能验证/筛选的全链路技术平台。其中RNA抗原包括针对羊驼进行RNA结构和序列优化的RNA;抗体发现与抗体工程服务采用噬菌体展示、RNA以及哺乳动物细胞展示在内的多种技术路线。通过多平台的交叉互补为药企及科研院所提供灵活的抗体发现及改造服务,助力药物试剂的研发。
除纳米抗体天然文库外,纳博生命科技还推出了现货免疫库,帮助客户快速筛选符合需求的抗体分子。
联系方式:400-822-9180 丨 联系邮箱:marketingdept@nanobodylife.com