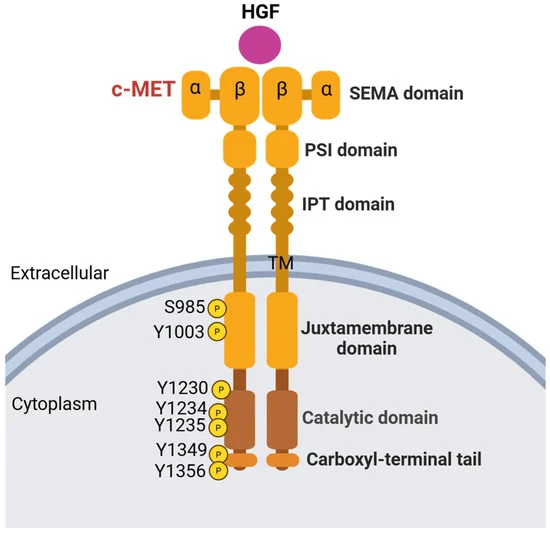
图1:c-MET/HGFR的结构和功能域 [1]
c-MET靶点的核心应用领域
基于c-MET靶点的作用机制,其目前的靶向治疗的核心应用领域为肿瘤治疗及诊断领域,部分研究已将其潜力拓展至心血管疾病及炎症性心肌炎治疗领域,但均属基础研究。
在肿瘤治疗领域内,其核心应用场景覆盖非小细胞肺癌、肝细胞癌、胃癌、结直肠癌、胶质母细胞瘤等,适配单靶点抑制剂、双抗、ADC、PROTAC等多技术路线,也用于克服EGFR-TKI耐药。而在肿瘤诊断方面则常用于筛选MET异常患者,如PET探针可实现MET表达的在体成像,助力患者分层,指导用药与疗效监测。
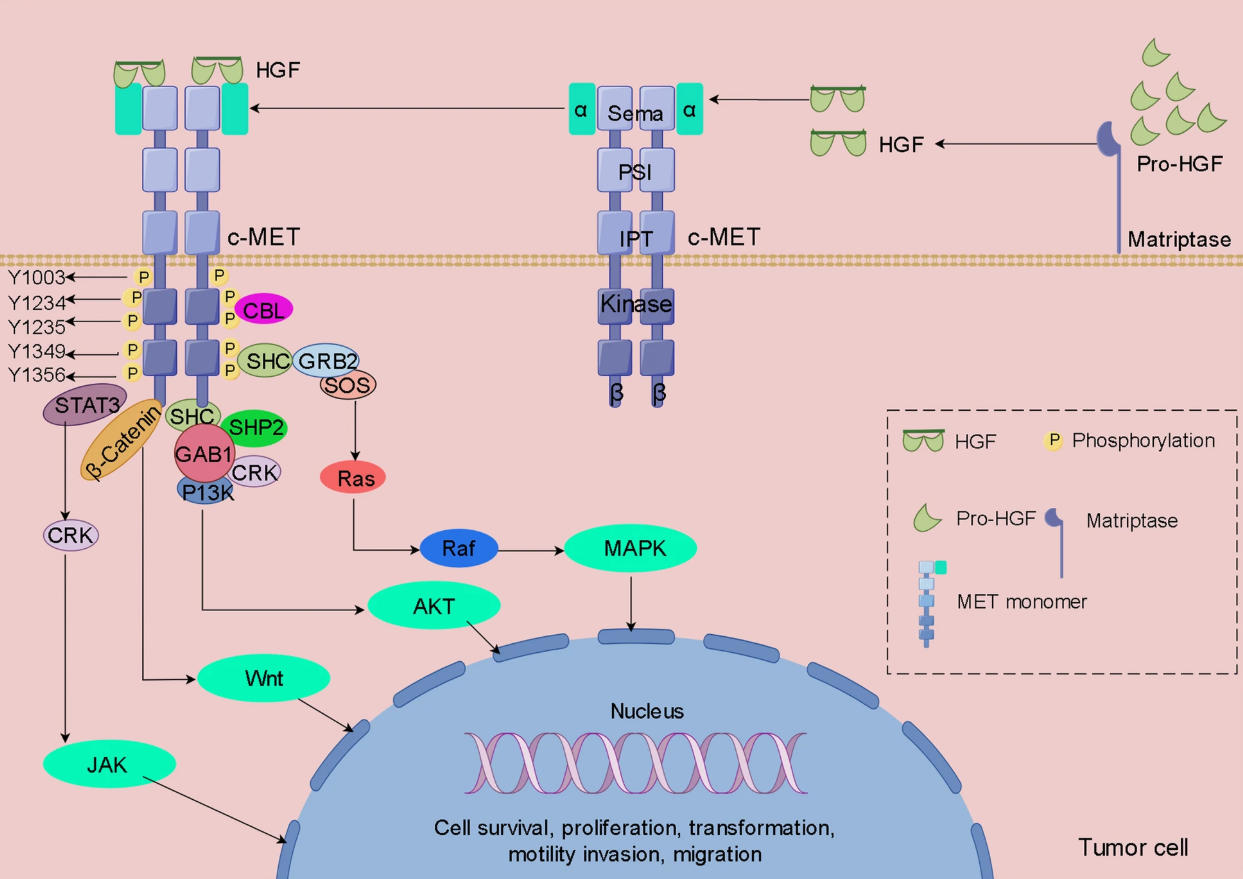
图2:c-MET/HGFR的信号通路网络 [2]
c-MET药物研发现状与领域最新进展
目前全球范围内,c-MET的靶向药物研究集中在肿瘤学领域,针对非肿瘤疾病开发的c-MET靶向药物的研究极少,且几乎没有进入临床阶段的成药研究案例。其作为一个在肿瘤领域已被临床验证的关键靶点,尤其在非小细胞肺癌的治疗和克服耐药中地位显著。据报道,全球已有超过200项c-MET管线在研,其技术路径涵盖了小分子、单/双/多抗、ADC等多种形式。已上市的c-MET/HGFR药物共计6款,以小分子抑制剂为主,其次为双特异性抗体与ADC药物,而已进入临床后期的c-MET/HGFR在研药物与已上市药物的作用机制则基本相似。
- 选择性小分子抑制剂(TKI)类:特泊替尼(Tepotinib)、卡马替尼(Capmatinib)、赛沃替尼(Savolitinib)、谷美替尼(Glumetinib)及伯瑞替尼(Bozitinib);
此类药物核心机制为竞争性阻断c-MET与ATP结合,抑制受体二聚化及自磷酸化,阻断PI3K/AKT、RAS/MAPK等促肿瘤通路;同时诱导异常c-MET受体溶酶体降解,降低膜表面功能受体水平,精准抑制MET ex14跳变、扩增/过表达肿瘤,安全性良好。其差异点在于,特泊替尼、伯瑞替尼穿透血脑屏障,适配脑转移患者;赛沃替尼对MET扩增/过表达肿瘤针对性更强,抑血管生成作用突出。
- EGFR/c-MET双特异性抗体类:埃万妥单抗(Amivantamab);
埃万妥单抗是一种全人源IgG 1型EGFR/c-MET双特异性抗体,其通过“信号阻断+受体降解+免疫杀伤”三重协同起效。两端分别结合EGFR与c-MET胞外域,阻断配体结合及受体激活,抑制双通路并克服MET介导的EGFR-TKI耐药;诱导受体异源二聚体内吞降解,降低膜受体密度;Fc段激活NK细胞ADCC、巨噬细胞ADCP等免疫效应,实现靶向与免疫协同杀伤。
- C-MET ADC药物:特立妥珠单抗(Telisotuzumab Vedotin,Emrelis);
作为全球首款获批的c-MET ADC药物,特立妥珠单抗由抗c-MET单抗、可裂解连接子及MMAE载荷组成。单抗靶向结合c-MET后随细胞内吞,溶酶体环境下连接子裂解释放MMAE;MMAE破坏微管平衡,阻断细胞分裂,诱导c-MET高表达肿瘤细胞凋亡,实现精准杀伤并降低脱靶毒性。
纳米抗体在c-MET抗体药物研发中的优势
目前公开的c-MET/HGFR靶向药物研发中,纳米抗体技术路径仍处于早期探索阶段,但由于纳米抗体具备更强的组织穿透性与病灶可达性、更优的内吞效率与靶向递送能力、更灵活的分子改造与多靶点构建能力、更高效的生产与成本优势及更稳定的理化特性等独特优势,被科研人员认为具有高度的应用价值。
如:浙江科弈药业通过专利申请公开了一类靶向c-MET的特异性纳米抗体及基于该抗体构建的药物偶联物(NADC),专利文献显示其纳米抗体具备分子量小、肿瘤组织渗透快、内吞活性高的特点,相比传统药物可更高效将细胞毒性载荷递送至c-MET阳性肿瘤细胞内,为c-MET相关肿瘤治疗提供了新的靶向递送方案。此外,北京星亢原生物开创了全球首款EGFR×c-MET双特异性纳米抗体偶联药物HNXV11,该药物通过免疫文库筛选出EGFR和c-MET纳米抗体后将二者异二聚化构建成含Fc段的双特异性纳米抗体,并采用双特异性纳米抗体+可裂解连接子+细胞毒性载荷(MMAE或DXD)的结构设计形成NADC。体外实验显示HNXV11对c-MET和EGFR胞外域的结合亲和力分别达2.94 nM和14.8 nM,可强效抑制c-MET和EGFR的磷酸化;在携带EGFR突变和野生型c-MET的H1975非小细胞肺癌模型中,HNXV11-MMAE或HNXV11-DXD均表现出强效抗肿瘤活性,且未观察到体重下降等明显毒性;同时,HNXV11在H1975、KYSE70等细胞系中展现出优于埃万妥单抗类似物的抗体依赖的细胞毒性效应,且内吞活性优异。
研究证实,相较于传统c-MET靶向药物技术路径,纳米抗体的独特优势在诸多抗体药物的成药研发中具备传统药物无可比拟的优势,其穿透性使之更易抵达实体瘤深部及脑部病灶,能精准解决传统药物靶向性不足、递送效率低等痛点。同时,纳米抗体结构稳定、改造灵活使其生产成本更低。
纳博生命拥有的pDual噬菌体展示技术,能够在传统噬菌体展示的高效开发的基础上,无缝连接哺乳动物细胞高效生产,大大提高筛除问题分子的效率;而NabLib®哺乳动物细胞展示技术,不仅可以提升筛选分子的可开发性,还可以灵活地选择抗体的筛选构型,为下游抗体分子的应用和检测提供更好的保障。